Humanos tienen los mismos genes que los animales que hibernan, lo que podría revolucionar el tratamiento de enfermedades
Un estudio realizado por genetistas estadounidenses sugiere que los genes de las especies que hibernan permanecen latentes en nuestro interior. Si logramos descubrir cómo funcionan, podríamos curar enfermedades como la diabetes y el Alzheimer.

Para sobrevivir durante meses sin comida ni agua, los animales que hibernan desafían todas las limitaciones biológicas. Sus músculos no se atrofian, su temperatura corporal desciende a casi cero, mientras que su cerebro y metabolismo se ralentizan drásticamente.
Estas capacidades han fascinado a los investigadores desde hace mucho tiempo, pero hasta ahora nadie se había preguntado si los humanos podíamos hacer lo mismo. Esa es la hipótesis que ha planteado un equipo de investigadores de la Universidad de Utah (Estados Unidos).

El estudio publicado en la revista Science sugiere que, aunque oculta en nuestro cuerpo, también llevamos esta resiliencia en nuestro ADN. En otras palabras, los genes que impulsan la hibernación, que hasta ahora parecían exclusivos de los reinos animal y vegetal, podrían estar latentes en nuestro interior.
Comprender y desentrañar sus mecanismos podría representar un avance revolucionario en el tratamiento de enfermedades crónicas y neurodegenerativas.
Anatomía de la hibernación
Para desentrañar el mecanismo de hibernación, los científicos se centraron en un conjunto de genes FTO (del inglés fat mass and obesity associated – asociado a la masa grasa y la obesidad). Los animales que hibernan lo utilizan para controlar el almacenamiento de grasa y energía durante el invierno.
Para los humanos, esta secuencia específica de ADN constituye un factor de riesgo genético más importante para la obesidad. Sin embargo, en animales que hibernan, esta región sirve para activar o desactivar la actividad genética.
Lo que estos controladores hacen no es alterar los genes en sí, sino regular su comportamiento, actuando como un director de orquesta que ajusta el volumen y la intensidad.
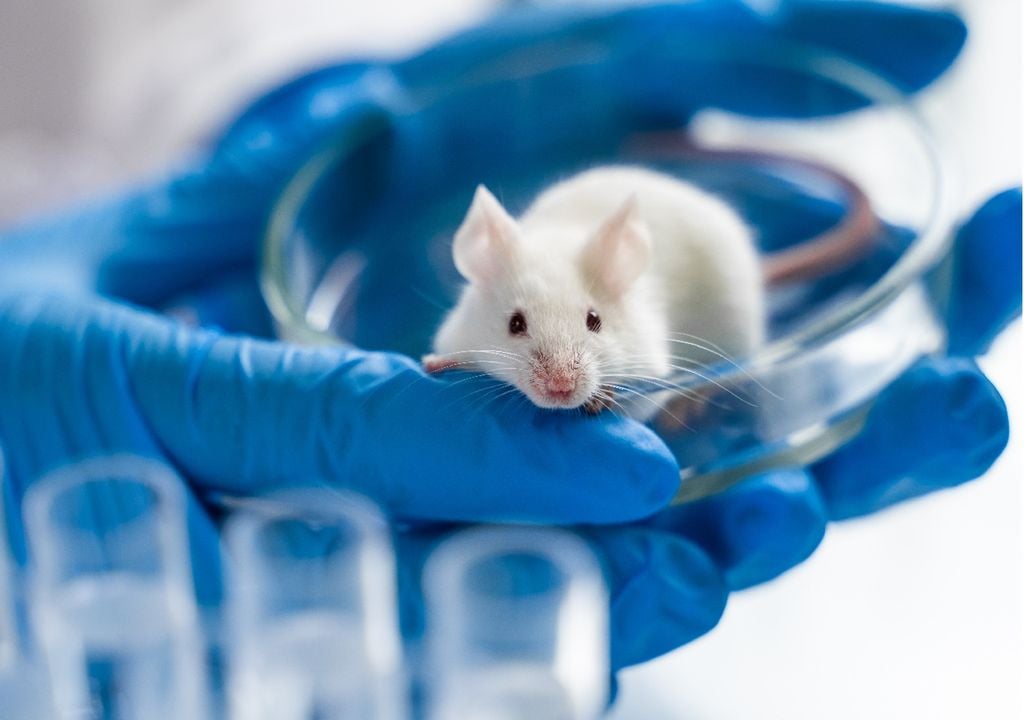
Al insertar los grupos de genes FTO en el ADN de ratones, los resultados mostraron que algunos aumentaron o perdieron peso según la dieta. Otros también mostraron cambios en la recuperación de la temperatura corporal o el metabolismo.

"Cuando eliminamos uno de los elementos de esta pequeña y aparentemente insignificante región del ADN, la actividad de cientos de genes cambia", explicó Susan Steinwand, coautora del estudio, citada en el comunicado de la Universidad de Utah.
Desinhibidores del metabolismo
Estos reguladores de ADN no crean genes. En cambio, eliminan los obstáculos que limitan la flexibilidad metabólica. Los científicos sospechan que los animales que hibernan podrían haber evolucionado para perder este tipo de restricciones.
La principal diferencia entre los humanos y los animales que hibernan podría residir, entonces, en cómo se regula este conjunto de genes. Esta capacidad también podría significar que algún día podríamos ajustar nuestro metabolismo de forma similar.
Adaptación biológica
Para encontrar estas pistas genéticas, el equipo de genetistas buscó primero regiones de ADN que se han mantenido estables en la mayoría de los mamíferos durante más de 100 millones de años, pero que han mostrado cambios drásticos recientes en las especies que hibernan. Existe evidencia sólida de que estos cambios repentinos en el ADN son resultado de adaptaciones específicas al comportamiento de hibernación.
Una vez identificados estos grupos de genes, los investigadores estudiaron ratones en ayunas. El ayuno refleja ciertas condiciones biológicas observadas en la hibernación, como una ingesta energética reducida y un metabolismo más lento.
El equipo identificó los genes que se activaron o desactivaron durante este período y mapeó los llamados “centros” que son responsables de ajustar las redes reguladoras genéticas más amplias.
Curiosamente, muchas de las regiones alteradas en animales que hibernaban se encontraban cerca de estos genes centrales. Estas superposiciones indican que los cambios evolutivos podrían haber modificado los interruptores de control genético para favorecer la hibernación.
Estos elementos reguladores identificados parecen ser cruciales para coordinar las funciones metabólicas y neurológicas y, según los autores del estudio, ahora son objetivos clave para futuras investigaciones genéticas.
Aprendiendo de los animales
En lugar de inventar nuevos rasgos, la evolución en animales que hibernan podría haber superado obstáculos metabólicos. Si bien los humanos aún no tienen estos obstáculos, sus genes poseen las mismas herramientas básicas.
Esto significa que, al tener una estructura genética idéntica a la de estas especies, sólo necesitamos identificar los interruptores de control para activar estas características típicas de los animales que hibernan.

Los hallazgos podrían ser un punto de partida para futuras investigaciones, abriendo innumerables posibilidades para la medicina y la genética. Si identificamos y aprovechamos estos interruptores reguladores, podríamos encontrar nuevas maneras para que los humanos sobrevivan al estrés metabólico extremo, reviertan el deterioro asociado con el envejecimiento o traten enfermedades crónicas.
Comprender los procesos genéticos relacionados con la hibernación podría, por lo tanto, brindar la oportunidad de encontrar nuevos enfoques para el tratamiento de enfermedades degenerativas y metabólicas. Si estos mecanismos se encuentran ocultos en el genoma humano, debemos encontrar maneras de activarlos y aprender de quienes hibernan para mejorar nuestra propia salud.
Referencia de la noticia
Susan Steinwand, Cornelia Stacher Hörndli, Elliott Ferris, Jared Emery, Josue D. Gonzalez Murcia, Adriana Cristina Rodriguez, Riley J. Spotswood, Amandine Chaix, Alun Thomas, Crystal Davey & Christopher Gregg. Conserved noncoding cis elements associated with hibernation modulate metabolic and behavioral adaptations in mice. Science
No te pierdas la última hora de Meteored y disfruta de todos nuestros contenidos en Google Discover totalmente GRATIS
+ Seguir a Meteored